卫材在2022ESMO上公布海乐卫的事后分析结果
分析评价了艾立布林在三项临床研究中对转移性HER2低表达乳腺癌的疗效
卫材株式会社(总部:东京,首席执行官:内藤晴夫,“卫材”)公布了三项随机、关键性III期研究(EMBRACE试验/研究305、研究301和研究304)的事后分析结果,这三项研究旨在评价甲磺酸艾立布林(HALAVEN®,中文名:海乐卫®)与其它化疗(分别为医生选择的化疗药物[TPC]、卡培他滨和长春瑞滨)相比治疗HER2低表达或无HER2表达的转移性乳腺癌(mBC)患者的疗效。这些数据已于2022年9月9日至13日在法国巴黎举行的欧洲肿瘤内科学会(ESMO)年会(#ESMO22,线上线下结合)上以海报的形式呈现(报告:#259P)。
HER2低表达乳腺癌亚型是一种新定义的癌症类型,包括既往根据免疫组化(IHC)测定和原位杂交(ISH)测定结果评估为HER2阴性的肿瘤。HER2低表达肿瘤的HER2蛋白表达水平较低,但并不足够被认为是HER2阳性。HER2低表达定义为IHC评分为1+或2,且ISH评分为阴性。预计2022年美国约有28.8万新增女性乳腺癌确诊病例1。据估计,约有80-85%的患者以前被视为HER2阴性亚型患者,而其中约60%的患者现在将被视为HER2低表达亚型患者2。
卫材首席科学官兼高级副总裁Takashi Owa博士表示:“在这项事后分析中,HER2低表达mBC患者的结局与三项关键性III期临床试验的结果一致。随着肿瘤学界对mBC的认识的不断深入,继续评价现有疗法在新疾病背景下的作用,以此帮助医疗保健专业人员完善知识体系也变得越来越重要。”
事后分析数据
事后分析包括三项试验的数据,即艾立布林相较于TPC(NCT00388726,EMBRACE试验/研究305)、卡培他滨(NCT00337103,研究301)以及长春瑞滨(NCT02225470,研究304)治疗既往接受过化疗(包括蒽环和紫杉烷类药物)治疗(研究301≤2线;研究304和EMBRACE试验/研究305为2-5线)的局部复发性或转移性乳腺癌患者。EMBRACE试验/研究305、研究301和研究304共入组1589名符合条件的患者,所有研究中各治疗组之间的基线特征基本均衡。对中位总生存期(OS)、中位无进展生存期(PFS)和客观缓解率(ORR)进行了分析。PFS和ORR由独立影像学审查委员会根据实体瘤疗效评价标准(RECIST)(1.0版:EMBRACE试验/研究305和研究301;1.1版:研究304)进行测量。ORR则在可评价患者(EMBRACE试验/研究305)和意向治疗人群(研究301和研究304)中进行测量。
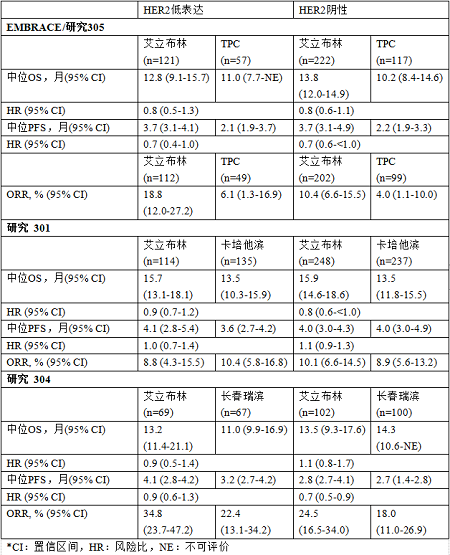
在事后分析中,HER2低表达或HER2阴性患者的OS、PFS和ORR总体上与EMBRACE试验/研究305、研究301和研究304中艾立布林治疗组的结果相似3,4,5。这三项研究中HER2低表达和HER2阴性患者的疗效结果总结见下表:
-
 北京耀中成功举办DSE课程说明会
北京耀中成功举办DSE课程说明会 -
 银轮股份:站上液冷风口,“千亿事业”有望加速实现
银轮股份:站上液冷风口,“千亿事业”有望加速实现 -
 ETC最新重要报告全面介绍全球建筑业排放状况和脱碳路径
ETC最新重要报告全面介绍全球建筑业排放状况和脱碳路径 -
 Assembly任命Karen Ho为大中华区董事总经理,引领该地区增长
Assembly任命Karen Ho为大中华区董事总经理,引领该地区增长 -
 Quantinuum宣布具巨大商业潜力的生成式量子人工智能突破
Quantinuum宣布具巨大商业潜力的生成式量子人工智能突破 -
 AI 与基因组学进步为亚洲肺癌负担带来新希望
AI 与基因组学进步为亚洲肺癌负担带来新希望 -
 E Ink元太科技发布75吋E Ink Kaleido™ 3户外大型彩色电子纸广告牌
E Ink元太科技发布75吋E Ink Kaleido™ 3户外大型彩色电子纸广告牌 -
 布鲁可携多IP系列产品亮相德国纽伦堡玩具展,持续推进全球化战略布局
布鲁可携多IP系列产品亮相德国纽伦堡玩具展,持续推进全球化战略布局 -
 森林城市再迎重磅利好,数字地位赋能区域发展
森林城市再迎重磅利好,数字地位赋能区域发展 -
 IBM 发布 2024 年第四季度业绩报告:软件业务双位数增长,自由现金流超全年预期
IBM 发布 2024 年第四季度业绩报告:软件业务双位数增长,自由现金流超全年预期